W środę, 20 marca 2026 roku, Główny Inspektor Farmaceutyczny wydał decyzję nr 18/WC/ZW/2026, która ma istotne znaczenie dla sektora ochrony zdrowia w Polsce oraz branży farmaceutycznej.
Decyzja GIF dotycząca leku Curosurf
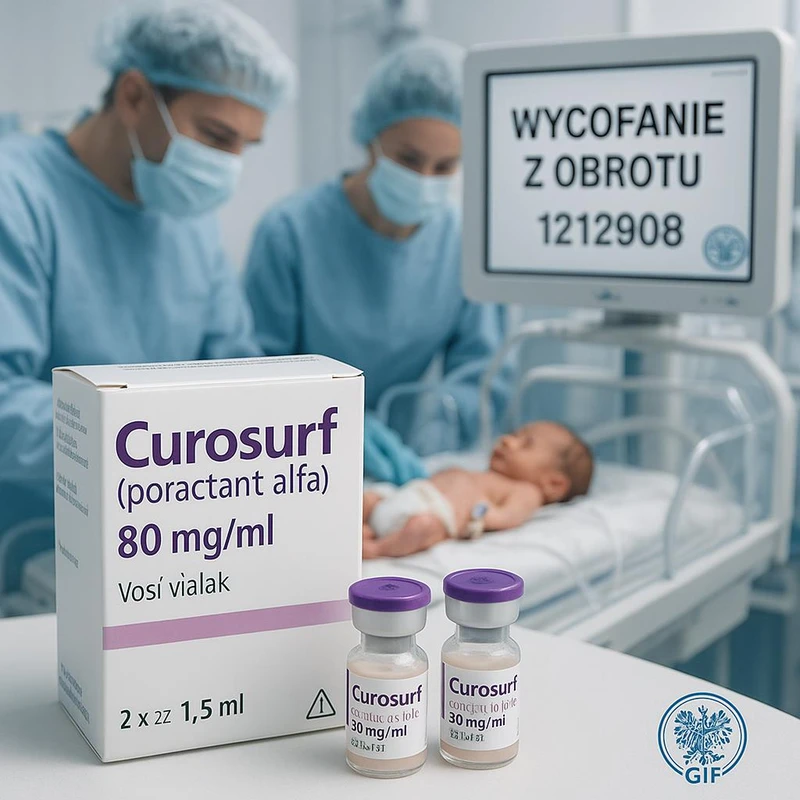
Dotyczy ona produktu leczniczego Curosurf (Poractant alfa 80 mg/ml), stosowanego dotchawicznie i dooskrzelowo, głównie u wcześniaków i noworodków z zaburzeniami surfaktantu.
Produkt był dostępny w opakowaniach zawierających dwie fiolki po 1,5 ml (GTIN 05909991395858) i trafiał na polski rynek w ramach importu równoległego.
Decyzja GIF obejmuje zakaz wprowadzania do obrotu oraz natychmiastowe wycofanie określonych serii leku.
Ryzyko skażenia mikrobiologicznego
Podstawą decyzji były informacje pochodzące z międzynarodowego systemu Rapid Alert oraz dane przekazane przez:
-
czeski Państwowy Instytut Kontroli Leków (SÚKL),
-
włoską Agencję Leków (AIFA).
Zebrane raporty wskazują na potencjalne skażenie mikrobiologiczne wykryte w ramach monitoringu środowiskowego (EM). Choć serie przeszły formalny proces zwolnienia do obrotu, producent – Chiesi Farmaceutici S.p.A. – zdecydował się na ich wycofanie w celu minimalizacji ryzyka dla pacjentów.
Serie objęte wycofaniem
Decyzja dotyczy konkretnych serii produktu, które były dystrybuowane m.in. w Rumunii i Bułgarii, a następnie trafiły do Polski w ramach importu równoległego (pozwolenie nr 85/19).
Wycofaniu podlegają następujące serie:
-
1212908 (termin ważności: 31.07.2026)
-
1224254 (termin ważności: 31.03.2027)
-
1210982 (termin ważności: 31.07.2026)
-
1204160 (termin ważności: 30.04.2026)
Podmiotem odpowiedzialnym za dystrybucję w Polsce jest Delfarma Sp. z o.o. z Łodzi, działająca na podstawie zezwoleń nr 85/19 oraz 211/24.
Rygor natychmiastowej wykonalności
Decyzji nadano rygor natychmiastowej wykonalności na podstawie art. 108 § 1 Kodeksu postępowania administracyjnego. Oznacza to, że działania muszą zostać podjęte niezwłocznie – bez oczekiwania na zakończenie procedury odwoławczej.
Uzasadnieniem jest bezpośrednie zagrożenie dla zdrowia i życia pacjentów, szczególnie noworodków, dla których nawet niewielkie odchylenia jakościowe mogą mieć poważne konsekwencje.
Znaczenie dla szpitali i personelu medycznego
Placówki medyczne, zwłaszcza oddziały neonatologiczne, powinny natychmiast:
-
zweryfikować stany magazynowe,
-
zidentyfikować wskazane serie,
-
wycofać je z użycia,
-
zabezpieczyć produkty przed ponownym wprowadzeniem do obrotu.
Ważne jest również sprawdzenie unikalnych identyfikatorów (L2I) zgodnie z wymogami Dyrektywy 2016/161 dotyczącymi zabezpieczeń leków.
W przypadku braku dostępności Curosurf konieczne może być zastosowanie alternatywnych terapii surfaktantowych, jeśli są dostępne w danej placówce.
Kontekst międzynarodowy i system nadzoru
Sprawa pokazuje znaczenie współpracy międzynarodowej w nadzorze nad bezpieczeństwem leków. Dane z Czech i Włoch oraz analiza retrospektywna wyników badań mikrobiologicznych były kluczowe dla podjęcia decyzji.
Systemy takie jak:
-
Rapid Alert,
-
monitoring środowiskowy (EM),
stanowią fundament szybkiego reagowania na potencjalne zagrożenia w łańcuchu dostaw.
Obowiązki dystrybutorów i importerów
W przypadku importu równoległego szczególne znaczenie ma:
-
prawidłowe oznakowanie opakowań,
-
zgodność z systemami weryfikacji,
-
skuteczne wycofywanie produktów z rynku.
Decyzja GIF przewiduje również możliwość zniszczenia wadliwych produktów, bez możliwości ich ponownego wykorzystania.
Znaczenie dla pacjentów i systemu ochrony zdrowia
Dla pacjentów i ich rodzin decyzja jest dowodem skutecznego działania systemu ochrony zdrowia. Pokazuje, że:
-
bezpieczeństwo leków jest priorytetem,
-
procedury reagowania działają sprawnie,
-
ryzyko jest eliminowane na wczesnym etapie.
Podsumowanie – co należy zrobić?
Placówki medyczne powinny:
-
natychmiast sprawdzić zapasy,
-
wycofać serie: 1212908, 1224254, 1210982, 1204160,
-
skontaktować się z GIF w razie wątpliwości,
-
wdrożyć procedury zabezpieczające.
Wnioski dla branży farmaceutycznej
Decyzja nr 18/WC/ZW/2026 to wyraźny sygnał dla rynku:
-
konieczność ścisłego monitorowania jakości,
-
znaczenie międzynarodowej współpracy,
-
potrzeba szybkiego reagowania na potencjalne zagrożenia.
To przykład proaktywnej polityki zdrowia publicznego, która wzmacnia bezpieczeństwo pacjentów i standardy w całym systemie dystrybucji leków.